2019年2月1日,开云电子(中国)官方网站的子公司深圳市先健心康医疗电子有限公司(先健心康)收到国家药品监督管理局(NMPA)的正式书面通知,确认8301型临时起搏器进入创新医疗器械特别审批程序,即“绿色通道”。
创新医疗器械特别审批程序是NMPA鼓励和推进中国医疗器械研究与创新发展的一项重要支持性措施。自批准之日起,NMPA将安排专人为先健心康8301型临时起搏器提供注册评审问题沟通及指导,并在满足审评要求的情况下,对该创新产品予以优先办理。
临时起搏器是一种体外电子治疗仪器。它在治疗严重心律失常患者以及提供心动过缓临时起搏保护方面具有药物无法替代的临床价值。先健心康8301型临时起搏器是一款起搏/分析二合一的多功能产品,并对人机界面进行了优化。该产品获得了2018年德国红点设计奖。它既适用于为心动过缓患者提供单腔(心房或心室)体外临时起搏,又适用于在起搏器和除颤器植入手术中进行起搏系统分析。除此之外,该设备还可以连续测量起搏导联系统的阻抗和感知幅度,以及实时连续显示腔内心电图,非常适合主动电极导线植入后的损伤电流的临床观察。先健心康8301型临时起搏器的自主研制成功标志着开云电子(中国)官方网站继先健芯彤植入式起搏器上市后在心脏节律管理领域的产业化又迈出了坚实的一步。
目前,先健心康8301型临时起搏器在中国已进入临床阶段。本次临床试验邀请了中山大学附属第一医院为组长单位,并与南方医科大学南方医院、中山大学孙逸仙纪念医院等5家临床中心共同合作,预计在一年内完成。该产品的多中心临床试验研究者会已于2018年10月中旬在广州召开。首例临床入组也于2018年12月下旬在广州中山大学附属第一医院顺利完成,该设备在临床试验中表现良好。

(图1:8301型临时起搏器多中心临床研究者会)
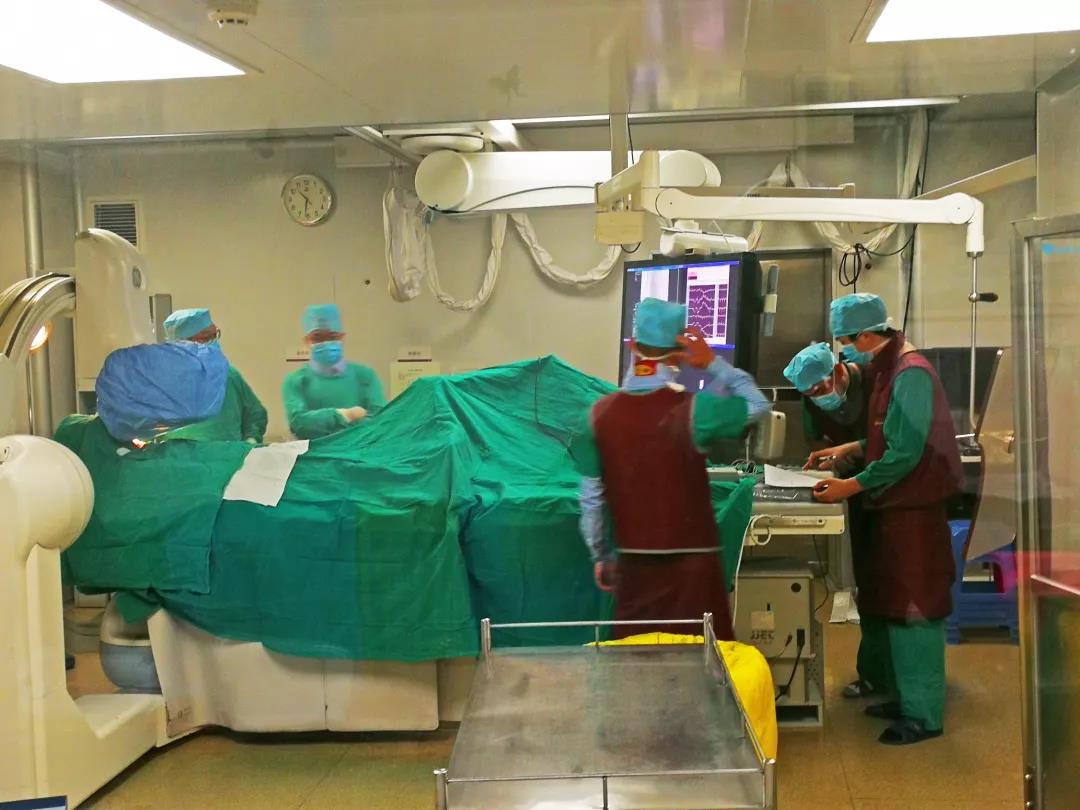
(图2:首例临床入组成功)
先健心康8301型临时起搏器功能全面并具有独创性,其各项功能设计均达到进口同类产品的水平,其部分性能指标和功能已经优于进口同类产品。该产品的上市,将填补我国国产临时起搏器的空白,并有望打破进口临时起搏器的垄断局面,为国内各级医疗机构提供质量上乘、功能齐全且更符合我国临床应用国情的国产临时起搏器。